Las obleas de SiC están disponibles para electrónica de potencia, aplicaciones científicas o industriales, con especificaciones como:https://www.powerwaywafer.com/sic-wafer/sic-wafer-substrate.html
SiC es un compuesto binario formado en una proporción 1:1 de elementos Si y C, que consta de 50% silicio (Si) y 50% carbono (C). Su unidad estructural básica es el tetraedro Si-C.
1. Disposición de la estructura cristalina de SiC
1.1 Estructura del tetraedro de Si-C
La energía del enlace Si-Si es de 310 kJ/mol, lo que puede entenderse como la fuerza necesaria para separar estos dos átomos. Cuanto mayor sea la energía de enlace, mayor será la fuerza necesaria para separarse. El espaciamiento atómico del enlace Si-C es 1,89 Å y la energía del enlace es 447 kJ/mol. A partir de la energía de enlace, se puede ver que, en comparación con los materiales semiconductores tradicionales a base de silicio, los materiales semiconductores a base de carburo de silicio tienen propiedades químicas más estables. En el gráfico se puede ver que cualquier átomo de C está conectado a los cuatro átomos de Si más cercanos, mientras que, a la inversa, cualquier átomo de Si está unido a los cuatro átomos de C más cercanos.
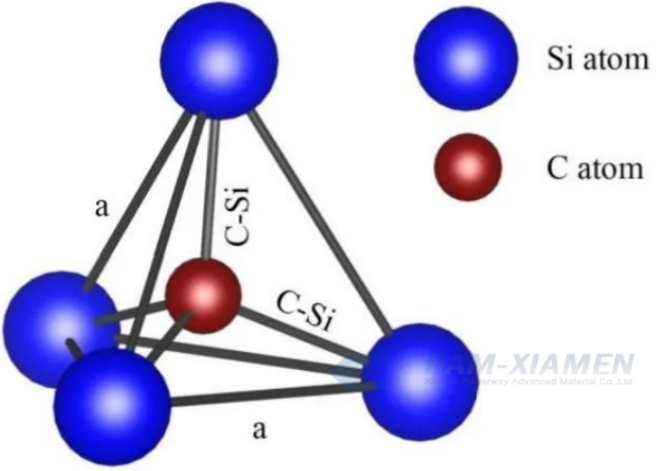
Fig. 1 Diagrama esquemático de la estructura tetraédrica de Si-C del cristal de SiC.
1.2 Estructura en capas de SiC
La estructura cristalina de SiC también se puede describir utilizando el método de estructura en capas, como se muestra en la Fig. 2. Varios átomos de C en el cristal ocupan sitios de red hexagonales en el mismo plano, formando una capa densa de átomos de C, mientras que los átomos de Si también ocupan sitios hexagonales. sitios de red en el mismo plano, formando una capa densa de átomos de Si. Cada C en la capa de empaquetamiento atómico de C está conectado al Si más cercano, y viceversa, la capa de empaquetamiento atómico de Si también es la misma. Cada dos capas adyacentes de átomos de C y Si forman una doble capa atómica de carbono-silicio. La disposición y combinación de los cristales de SiC son muy diversas y hasta ahora se han descubierto más de 200 formas de cristales de SiC.
Para distinguir las diferentes formas cristalinas de SiC, actualmente se utiliza principalmente el método de Ramsdell para el etiquetado. Este método utiliza una combinación de letras y números para representar las diferentes formas cristalinas de SiC. Las letras se colocan al final para indicar el tipo de celda de cristal. C representa la forma de cristal cúbica, H representa la forma de cristal hexagonal y R representa la forma de cristal rómbico. El número se coloca al principio para indicar el número de capas de capas diatómicas de Si-C en la unidad repetitiva básica. A excepción de 2H-SiC y 3C-SiC, todas las demás formas cristalinas pueden considerarse como una mezcla de estructuras de esfalerita y wurtzita, es decir, una estructura hexagonal densamente empaquetada.
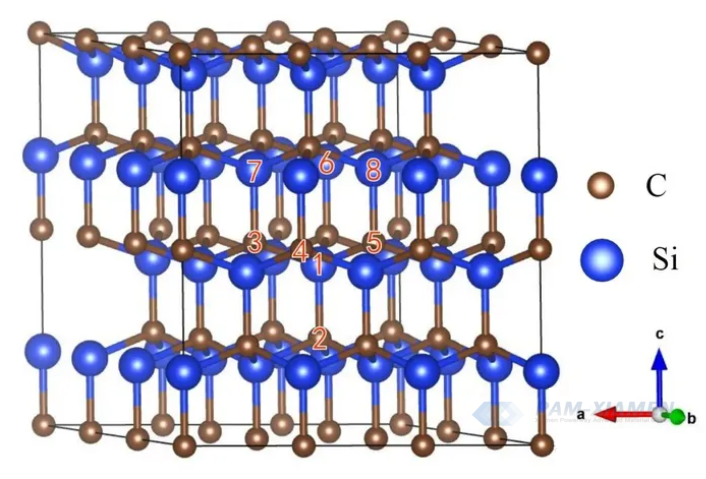
Fig. 2 Estructura en capas de cristal de SiC
2. ¿QuéAre C-Pcarril y si-PAGcarrilde la oblea de carburo de silicio?
El plano C se refiere al plano cristalino (000-1) de una oblea de SiC, que es la superficie cortada por el cristal a lo largo de la dirección negativa del eje c. El átomo terminal en esta superficie son los átomos de carbono. La superficie de silicio se refiere al plano cristalino (0001) de una oblea de carburo de silicio, que es la superficie cortada a lo largo de la dirección positiva del eje c del cristal. El átomo terminal de esta superficie son los átomos de silicio.
La diferencia entre el plano C y el plano de silicio puede afectar las propiedades físicas y eléctricas de las obleas de SiC, como la conductividad térmica, la conductividad, la movilidad del portador, la densidad de estados de la interfaz, etc. La selección del plano C y del plano Si puede También afectan el proceso de fabricación y el rendimiento de los dispositivos de SiC, como el crecimiento epitaxial, la implantación de iones, la oxidación, la deposición de metales, la resistencia de contacto, etc.
3. Aplicación de C-Pcarril y si-PAGcarrilde oblea de SiC
Durante el proceso de crecimiento de los cristales de SiC, debido a las diferencias en la densidad de disposición atómica y la estabilidad química entre las superficies de Si y C, exhiben diferentes características en el procesamiento de materiales y la preparación de dispositivos.
La cara de Si suele tener una mejor movilidad de los electrones y es adecuada como capa de canales para dispositivos electrónicos de potencia.
Mientras que la cara C puede presentar un mejor rendimiento, como una mayor conductividad térmica, en determinadas aplicaciones científicas o industriales específicas.
Para obtener más información, por favor contáctenos por correo electrónico avictorchan@powerwaywafer.comypowerwaymaterial@gmail.com.

