半導体材料として最も一般的に使用されている炭化ケイ素結晶は4H-SiCウェーハ。 ただし、炭化ケイ素結晶には複数の種類があります。 炭化ケイ素結晶成長の過程で条件が十分に制御されていない場合、結果として生じる炭化ケイ素結晶構造は、3C、6H、15Rなどである可能性がありますが、4Hではありません。
炭化ケイ素結晶の成長では、2つの側面を考慮する必要があります。
- SiC結晶自体の成長特性。 主な成長特性は、融点と分解点を含む相転移点です。 適切な結晶成長方法は、その成長特性に基づいて選択する必要があります。 大規模な炭化ケイ素の結晶成長に関しては、一般的な方法は、固液相変化を伴う液相法と、相状態によって分類される固気相変化を伴う気相法であり、このプロセスに参加した。 一般に、炭化ケイ素の成長プロセスでは固相法は使用されません。これは、純粋な固相-固相変態の欠点を克服することが難しいためです。
- 機器が耐えられる条件。 条件が満たされない場合、成長することは不可能です。 さらに、工業化された生産はコストを考慮しなければなりません。
炭化ケイ素結晶の特性は、状態図に基づいて分析できます(温度の変化やその他の延伸条件はあまり正確ではありません)。

通常の状態では、炭化ケイ素は液体になる前に分解しているため、液体状態の純粋な炭化ケイ素はSiC結晶成長プロセスに関与していません。 Siが過剰な場合、液相範囲は0.01%〜19%であり、液相法を使用することができます。 しかし、1700℃以上になると大量のSiが蒸発するため、単純な二元共晶成長技術ではSiC結晶成長を実現できません。
結論として、液相法に関連する炭化ケイ素単結晶成長の一般的な方法-均一溶融法は限られていますが、不均一溶融フラックス法(Si-C-Crのような3成分以上)はまだ開発中です。 液相法には4つの大きな利点があります。
- 直径の拡大;
- 厚くする;
- P型ドーピングが可能。
- 種結晶より1マグニチュード低い転位密度。
炭化ケイ素固体の昇華-昇華プロセス(2400-2500°C)が低温で実現できるのはおかしいです。これにより、昇華によって炭化ケイ素を成長させることができます。 昇華法は炭化ケイ素結晶を成長させる一種の気相法であり、ガスは固体の表面に結晶を形成します。
温度場のシミュレーションは、Virtual Reactor(SiC)ソフトウェアでシミュレートできます。 4H-SiCの成長に必要な種結晶温度は2120〜2200°C、空気圧は500〜3000Paです。 6H-SiC炭化ケイ素結晶の成長に必要な種結晶温度は2200〜2300°C、空気圧は1000〜10000Paです。
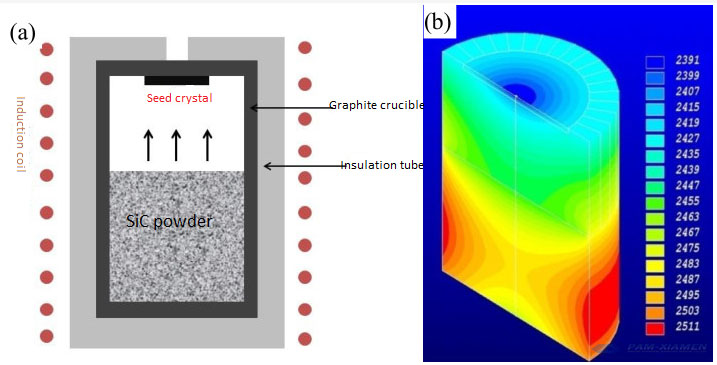
(a)炭化ケイ素結晶成長のためのPVT法
(b)PVT法で成長させたSiC結晶の内部温度場
高純度の半絶縁性6インチSiCを成長させるための理論的な温度場:種結晶温度は2200℃、成長圧力は30mbar、H2 + Ar雰囲気、厚さは22mmに達する可能性があります。
気相法は結晶を成長させます:
この方法の主なプロセスが化学反応であるかどうかは、物理蒸着と化学蒸着に分けることができます。
物理蒸着:
この方法の主なプロセスは物理的プロセスであり、化学反応は発生しません。 原料ガスは炭化ケイ素であり、得られる成長も炭化ケイ素です。 特定の機器を考慮に入れると、物理蒸着には昇華凝縮(物理蒸着、略してPVT)、真空蒸着、スパッタリング、イオンビーム蒸着、分子線エピタキシー、およびレーザー研磨が含まれます。 法律など。
化学蒸着(化学蒸着、CVDと呼ばれる)の場合、化学反応の生成を伴う必要があります。 同様に、化学蒸着には、気相エピタキシー、ホットフィラメント法、マイクロ波プラズマ化学蒸着、有機金属化学蒸着(MOCVD)などが含まれます。
例えば、GaAsはMOCVD法で成長させます。 典型的な実験方法は次のとおりです。
圧力は8kPa、温度は500-630°Cです。 原料はH2が運ぶTMGa / AsH3の混合ガスです。 このような条件下では、TMGa + AsH3 + H2が反応してGaAsを生成します。
同様に、炭化ケイ素は、物理蒸着と高温化学蒸着を使用して単結晶を成長させることができます。 下図のように、物理蒸着の原料は炭化ケイ素固体で、加熱すると気体になり、最終的に種結晶の表面で結晶になります(注:PVT法では種結晶が必要ですが、それ以外の場合はLelyメソッドです)。 ただし、化学蒸着は異なります。 原料はガスで、種結晶の表面で直接化学反応を起こし、結晶を形成します。
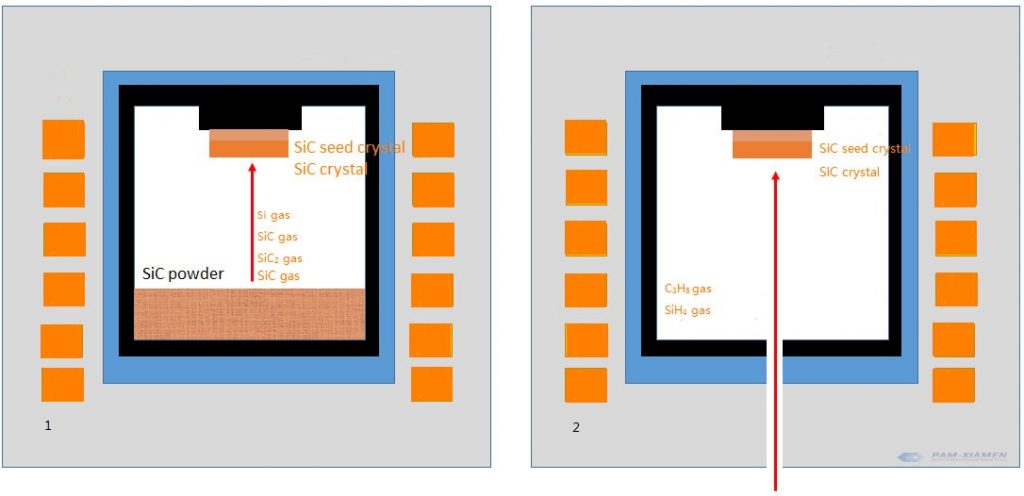
図1物理蒸着のPVT法
図2高温化学蒸着(HT-CVD)法
PVT法による炭化ケイ素の結晶成長は、複雑な物理的および化学的プロセスです。 高温での基本的な炭化ケイ素結晶成長プロセスには、原材料の分解と昇華、物質移動、種結晶の表面結晶化が含まれます。 物理的蒸気輸送による炭化ケイ素の成長には、2つの固有の特性があります。
- 原料は炭化ケイ素固体であるため、純度の管理は容易ではありません。
- 粉末をガスに変える過程で、さまざまなガスが発生する可能性があります。
固体のSiC粉末は分解し、昇華していくつかの異なる気相成分になります。 主なガス成分は、Si、SiC、Si2C、およびSiC2です。 反応式は以下の通りです。 グラファイトるつぼ内のCはSi蒸気と反応して、SiC2とSi2Cを生成します。 また、気相組成には少量のC、C2、Si2、Si3、Si2C3などが含まれますが、無視してかまいません。
SiC(s)= Si(g)↑+ C(s)
2SiC(s)= Si2C(g)↑+ C(s)
2SiC(s)= SiC2(g)↑+ Si(l、g)↑
SiC(s)= SiC(g)↑
C(s)+ Si(l、g)= SiC(s)
SiC原料の分解過程では、原料の昇華が不均一であるため、気相組成中のSi原子の数はC原子の数よりはるかに多くなります。 非化学量論比が高いと、SiとCが分離します。Siは気相に蓄積し、Cは固相に凝集します。 成長材料は、現時点で厳しく黒鉛化されます。 理論的には、成長界面近くでSi:Cの比率を1:1に保つことが最も理想的な成長方法ですが、これは実際の炭化ケイ素結晶成長プロセスで比率を維持することは困難です。 このため、化学量論比は、成長材料に適切な量のSiを添加して、過剰なCのバランスをとることによって維持できます。
Si、SiC、Si2C、SiC2ガスが種結晶の表面に到達すると、準安定領域で結晶が連続的に形成されます。
SiC(g)= SiC(s)
Si(g)+ SiC2(g)= 2SiC(s)
Si2C(g)+ SiC2(g)= 3SiC(s)
したがって、成長した炭化ケイ素単結晶の欠陥は、制御するためのより技術的な手段を必要とし、それは一般に導電性SiC基板を製造するために使用されます。
化学蒸着法は、原料として特殊ガスを使用するため、コストが高くなります。 現在では、半絶縁性SiC基板の製造にのみ使用できます。 2つの典型的な化学反応経路は次のとおりです。
C2H(g)+ 2SiH4(g)— 2SiC(s)+ 6H2(g)
3SiH4(g)+ C3H8(g)— 3SiC(s)+ 10H2(g)
SiH4のみを使用すると、V(Si):V(H2)> 0.05%のときにSi液滴が形成されます。 次に、ハロゲンを原材料に導入することで、Siの欠陥を減らすことができます。 使用されるタイプには、HCl、SiCl4、SiHCl3、CH3Cl、SiCl3H3、およびSiH3Clが含まれます。
必要な機器は、水平ホットウォールCVD-VP508であり、意図的なドーピング成長ゾーン、意図しないドーピング成長ゾーン、加熱システム、冷却システム、真空システム、ガス供給システム、排気ガス処理システム、制御システム、および警報システムが含まれます。
炭化ケイ素結晶の成長手順には、基板(種結晶)の洗浄、真空下でのエッチング、そしてエピタキシャル成長が含まれます。
基板の準備と洗浄-基板を反応チャンバーに入れます-真空-基板の高温その場エッチング-SiCのエピタキシャル成長のために元のガスを注入します-実験は終了し、サンプルを取り出します
成長率:5-10um / h、標準プロセスは次のとおりです。
- Siソース:SiH4SiHCl3 SiCl4
- Cソース:CH4C2H6 C3H8 CCl4
- キャリアガス:H2、Ar
- 温度:1200-1800℃
- 空気圧:10-1000mbar
PS:1bar = 1atm = 100kPa、標準大気圧との比較が簡単
これは、炭化ケイ素結晶成長の主な方法であり、PVT法とHTCVD法の2つの気相法です。
詳細については、メールでお問い合わせください。victorchan@powerwaywafer.comそしてpowerwaymaterial@gmail.com.

